做好RIP-qPCR实验,应避免以下常见问题。1. RNA降解:RNA极易降解,因此在实验过程中应始终使用无RNase的试剂和耗材,并在冰上操作以维持低温环境。样本处理后应立即进行后续实验,避免长时间存储。2. 非特异性结合:使用特异性强的抗体进行免疫沉淀是关键。同时,设置适当的对照实验,如使用非特异性抗体作为阴性对照,有助于识别非特异性结合。3. 引物问题:引物设计不合理可能导致非特异性扩增或引物二聚体形成。应确保引物具有高特异性,并避免引物间存在互补序列。4. 污染问题:实验过程中应严格避免RNA酶和其他污染物的引入。使用洁净的实验台和消毒的器具,实验人员应穿戴实验服和手套。5. 数据解读错误:在数据分析时,应注意识别并排除异常值。同时,使用适当的统计方法,确保结果的准确性和可靠性。对于不符合预期的结果,应进行重复实验以验证其真实性。通过避免这些常见问题,可以较大程度提高RIP-qPCR实验的成功率和准确性。在实验过程中,始终保持谨慎和细致的态度,遵循实验规范,是获得可靠结果的关键。RIP-qPCR实验技术是一种强大的研究RNA与蛋白质相互作用的方法,也存在一些不足之处。内蒙古RNA蛋白互作检测RIP Seq
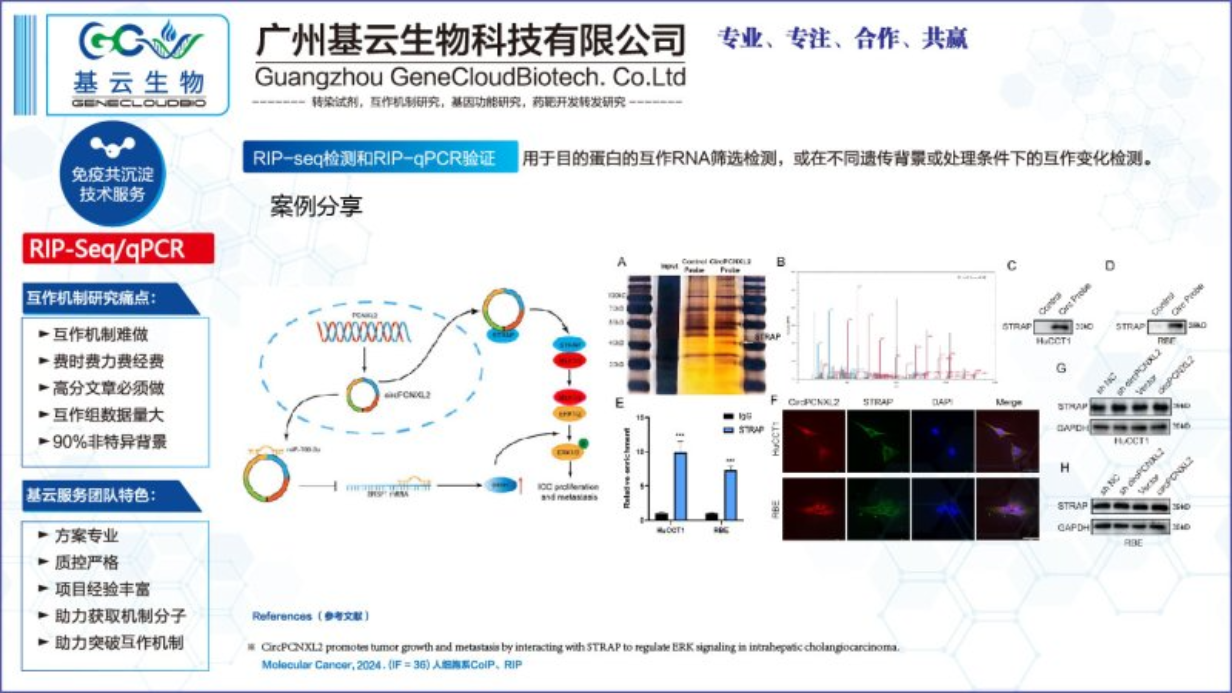
RIP-qPCR实验的基本实验流程如下:细胞裂解:收集目标细胞,使用适当的裂解液进行裂解,释放细胞内的RNA和蛋白质。抗体结合:向细胞裂解液中加入特异性抗体,该抗体能与目标蛋白质结合,形成抗体-蛋白质复合物。免疫共沉淀:加入蛋白A/G磁珠或其他亲和树脂,与抗体-蛋白质复合物结合,然后利用磁力沉淀复合物,去除非特异性结合的蛋白质。RNA提取:从沉淀的复合物中提取RNA,此过程中应使用RNase抑制剂以保护RNA的完整性。逆转录:使用逆转录酶将提取的RNA逆转录为cDNA。qPCR反应:准备qPCR反应液,包括PCR缓冲液、dNTPs、酶、引物和探针等,将cDNA作为模板加入到反应液中,进行qPCR反应。通过反应,可以定量检测与目标蛋白质结合的特定RNA。数据分析:分析qPCR的结果,包括RNA的表达水平和与目标蛋白质的结合强度等。以上流程供参考,实际操作中可能需要根据实验需求进行适当的调整和优化。广东RNA免疫沉淀RIP-qPCR检测RIP-qPCR实验技术有哪些优缺点。
RIP-qPCR实验(RNA Immunoprecipitation followed by quantitative PCR)是一种用于研究细胞内特定蛋白质与RNA相互作用的技术。该技术结合了免疫沉淀(Immunoprecipitation)和实时荧光定量PCR(quantitative PCR,qPCR)的方法,旨在识别和定量与特定蛋白质结合的RNA分子。在RIP-qPCR实验中,首先使用针对目标蛋白质的特异性抗体进行免疫沉淀,将与该抗体结合的蛋白质-RNA复合物从细胞裂解液中分离出来。随后,通过洗涤步骤去除非特异性结合的分子,保留与目标蛋白质特异性结合的RNA。接下来,从免疫沉淀复合物中提取RNA,并将其逆转录为cDNA。然后,利用特异性引物进行qPCR反应,以定量检测与目标蛋白质结合的特定RNA分子的丰度。通过比较不同样品中目标RNA的相对表达水平,可以评估蛋白质与RNA之间的结合强度和特异性。RIP-qPCR实验在生物学研究中具有广泛应用,可用于研究转录后调控、RNA转运、RNA稳定性以及非编码RNA与蛋白质相互作用等方面的问题。该技术为揭示细胞内基因表达调控的复杂网络提供了有力工具。
RIP-qPCR实验在特定情况下被广泛应用。首先,当研究者需要验证特定RNA与蛋白质之间的相互作用时,RIP-qPCR是一个理想的选择。通过该技术,可以精确地检测和定量与特定蛋白质结合的RNA,从而证实它们之间的直接联系。其次,RIP-qPCR实验在研究RNA结合蛋白的功能和调控机制方面具有重要应用。通过分析不同条件下RNA与蛋白质的结合情况,可以深入了解RNA结合蛋白在转录后调控、RNA稳定性、定位以及翻译等方面的作用。此外,当研究者对特定细胞类型或组织中的RNA-蛋白质相互作用感兴趣时,RIP-qPCR也是一个合适的方法。该技术可以用于研究特定生理或病理状态下RNA与蛋白质的结合模式,为疾病机制的解析和新药开发提供重要线索。总之,RIP-qPCR实验在验证RNA与蛋白质相互作用、研究RNA结合蛋白功能和调控机制以及探索特定细胞类型或组织中的RNA-蛋白质相互作用等方面具有广泛应用。它为科学家提供了一种灵敏、特异且定量的方法来研究细胞内复杂的RNA-蛋白质相互作用网络。RIP和ChIP实验在研究对象、实验原理、实验操作、优化条件和技术应用等方面存在明显差异。

RIP-qPCR实验技术具有多个优点和一些潜在的缺点。优点:特异性高:RIP-qPCR结合了免疫沉淀和qPCR技术,能够特异性地识别并结合目标RNA结合蛋白(RBP)及其结合的RNA,降低非特异性结合的可能性。灵敏度高:qPCR技术具有高灵敏度,能够检测到低丰度的RNA分子,使得RIP-qPCR能够准确测量细胞中RNA与蛋白质的相互作用。定量准确:通过实时监测荧光信号,RIP-qPCR可以对目标RNA进行精确定量,提供可靠的定量数据。应用范围大:RIP-qPCR技术适用于多种生物样本和实验条件,可用于研究不同细胞类型、组织或生物体中的RNA-蛋白质相互作用。缺点:技术复杂性:RIP-qPCR涉及多个步骤,包括细胞裂解、免疫沉淀、RNA提取、逆转录和qPCR等,操作相对复杂,需要经验丰富的实验人员。抗体依赖性:实验结果的准确性和特异性高度依赖于所使用的抗体的质量和特异性。非特异性抗体可能导致假阳性或假阴性结果。RNA易降解:RNA分子在操作过程中容易降解,特别是在不适当的实验条件下,如存在RNase污染或操作时间过长。综上所述,RIP-qPCR实验技术具有高特异性和灵敏度,能够准确测量RNA与蛋白质的相互作用,但操作复杂、抗体依赖性强、RNA易降解以及成本较高是其潜在的缺点。RIP-qPCR实验的基本实验流程是什么。内蒙古RNA蛋白互作检测RIP Seq
进行RIP实验时,抗体的选择是实验成功的关键之一,选择抗体时需要考虑几个要点。内蒙古RNA蛋白互作检测RIP Seq
RIP(RNA结合蛋白免疫沉淀)实验的优点。特异性高:RIP实验使用特异性抗体来沉淀RNA结合蛋白,可以精确地研究目标RNA与特定蛋白质的相互作用。灵敏度高:RIP实验可以检测到低丰度的RNA结合蛋白,适用于研究稀有或低表达的RNA与蛋白质的相互作用。可用于研究RNA加工和调控机制:RIP实验可以揭示RNA与蛋白质的相互作用,从而深入了解RNA的加工、稳定性和调控机制。与高通量技术结合:RIP实验可以结合microarray技术(称为RIP-Chip)进行高通量分析,从而更好地了解RNA与蛋白的互作情况。这种结合可以提高实验的通量和效率,使得研究人员能够在基因组范围内研究RNA与蛋白的相互作用。总之,具有高度的特异性和灵敏度,可用于研究RNA与蛋白质的相互作用机制。内蒙古RNA蛋白互作检测RIP Seq